Создание моноклональных антител привело к революционным достижениям в диагностике и лечении многих онкогематологических заболеваний. Здесь мы рассмотрим основные этапы от изобретения моноклональных антител до внедрения их в клиническую практику.
Способ получения моноклональных антител был предложен в 1975 г. учеными Георгом Кёлером и Цезарем Мильштейном. Они разработали методику получения клеточных гибридов — гибридом. Гибридомы (гибридные опухолевые клетки) образуются в результате слияния лимфоцитов, полученных от иммунизированных животных, с клетками множественной миеломы костного мозга, культивируемыми in vitro.
Необходимо отметить, что В-лимфоциты могут жить только в организме хозяина, а в искусственной питательной среде они быстро погибают. Длительное культивирование В-лимфоцитов вне организма невозможно. Наоборот, клетки плазмоцитарной опухоли (множественной миеломы) хорошо культивируются и размножаются in vitro.
В 1970-е годы немецкий иммунолог Георг Кёлер изучал генетическую изменчивость антител. Для исследования было необходимо изолировать клон антителообразующих клеток — плазмоцитов (производных В-лимфоцитов). С целью реализовать свой проект Кёлер отправился в Великобританию, в лабораторию Мильштейна, изучавшего клоны плазмоцитом, и они вместе разработали оригинальный подход к решению этой проблемы.
Ученые решили получить соматический гибрид нормальной антителопродуцирующей и опухолевой клеток. В случае успеха такой гибрид унаследовал бы от нормальной В-клетки способность к синтезу антител, а от опухолевой — способность к неограниченному и бесконтрольному росту. Это им удалось осуществить путем создания гибридомной технологии.
Схема получения первых моноклональных антител:
1. Мышам вводят специфический антиген, который вызывает продукцию антител против этого антигена.
2. Селезенку мышей удаляют и гомогенизируют для получения суспензии клеток. Эта суспензия содержит B-клетки, которые продуцируют антитела против введенного антигена.
3. Клетки селезенки затем смешивают с клетками миеломы, которые способны непрерывно расти в культуре, в них также отсутствует резервный путь синтеза нуклеотидов.
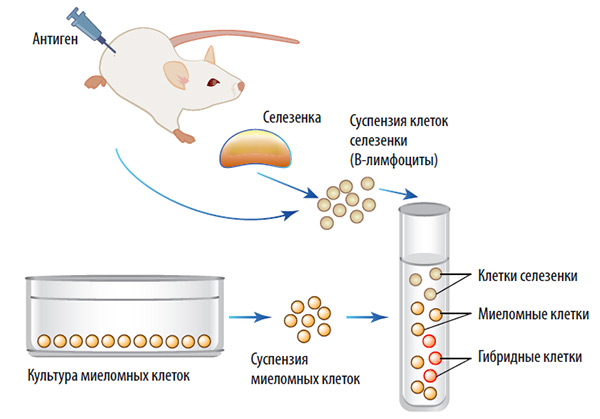
4. Некоторые антителопродуцирующие клетки селезенки и клетки миеломы сливаются, образуя гибридные клетки. Эти гибридные клетки теперь способны непрерывно расти в культуре и продуцировать антитела.
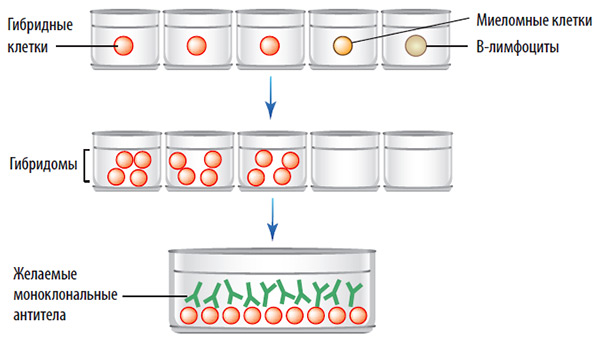
5. Смесь клеток помещают в селективную среду, которая позволяет расти только гибридным клеткам. Гибридные клетки пролиферируют, образуя клон гибридом.
6. Гибридомы проверяют на продукцию нужных антител.
7. Выбранные гибридомы затем культивируют для получения большого количества моноклональных антител.
Разработка технологии получения гибридом имела революционное значение в иммунологии, молекулярной биологии и медицине и позволила создать совершенно новые научные направления. Благодаря гибридомам возникли новые методы диагностики многих заболеваний и открылись новые пути для изучения злокачественных опухолей и многих других заболеваний. Ученые, разработавшие технологию получения моноклональных антител, в 1984 году стали лауреатами Нобелевской премии.
Моноклональные антитела в диагностике
Моноклональные антитела в силу своей высокой специфичности, стандартности и технологичности оказались исключительно удобным и широко применяемым в настоящее время диагностическим средством. С их помощью определяют маркеры клеточных популяций (фенотипирование клеток крови, в частности лимфоцитов), опухолевые маркеры, гормоны, медиаторы, любые молекулы, обладающие антигенностью.
Именно применение моноклональных антител в диагностике позволило значительно увеличить специфичность и чувствительность тест-систем, основанных на реакции антиген-антитело. Так, даже в простой реакции агглютинации моноклональные антитела (цоликлоны анти-А, анти-В и анти-D) применяют для определения агглютиногенов эритроцитов человека системы АВ0 и резуса. Они обладают высокой стандартностью и чувствительностью, характеризуются быстротой наступления и четкостью агглютинации.
Чрезвычайно важным стало использование иммунофенотипирования в онкогематологии. Иммунофенотипирование позволяет определить с помощью моноклональных антител наличие или отсутствие антигенов — кластеров дифференцировки (CD — cluster of differentiation) лимфоцитов, гранулоцитов и бластных клеток по представленным на клеточных мембранах молекулам-маркерам.
Многоцветная проточная цитометрия с использованием наиболее информативных комбинаций моноклональных антител позволила многосторонне изучать не только бластную популяцию, но и остаточные лимфоциты и гранулоциты с точки зрения их иммунофенотипических особенностей при различных опухолях системы крови.
Моноклональные антитела в терапии
Первые гибридомы были получены на основе В-лимфоцитов мыши, и поэтому моноклональные антитела по своей природе были мышиные. Этим обусловлено первостепенное их использование в лабораторной практике. Применение моноклональных антител в терапевтической практике было существенно ограничено, т.к. их введение человеку сопровождалось иммунным ответом на чужеродный мышиный белок.
Однако вскоре был разработан подход, значительно уменьшивший их иммуногенность при введении человеку и увеличивший лечебные возможности моноклональных антител. С помощью технологии рекомбинантных ДНК константные домены мышиных антител были заменены на соответствующие константные области иммуноглобулинов человека, и только вариабельные домены остались мышиными. Полученные таким способом моноклональные антитела принято называть химерными.
Химерные моноклональные антитела в своей структуре имеют более 65 % иммуноглобулина человека. Поскольку большая часть антигенных детерминант иммуноглобулинов находится в их константных доменах и с ними же связаны основные эффекторные функции, иммуногенность химерных иммуноглобулинов мышь/человек значительно снижена.
Следующим этапом с помощью трансгенных технологий стало создание гуманизированных моноклональных антител, которые на 95 % состоят из иммуноглобулина человека. В молекулах гуманизированных моноклональных антител мышиными являются только гипервариабельные участки CDR (complementarity-determining regions — регионы, определяющие комплементарность) — области Fab-фрагментов, которые ответственны за специфическое связывание антитела с антигенной детерминантой.
Развитие новых биотехнологий, в частности фагового дисплея, позволило полностью избежать использования мышей для создания полностью человеческих моноклональных антител. Такие антитела обладают самой низкой иммуногенностью при введении человеку. Таким образом, к настоящему времени получены мышиные, химерные, гуманизированные и полностью человеческие моноклональные антитела, что находит свое отражение в номенклатуре препаратов.
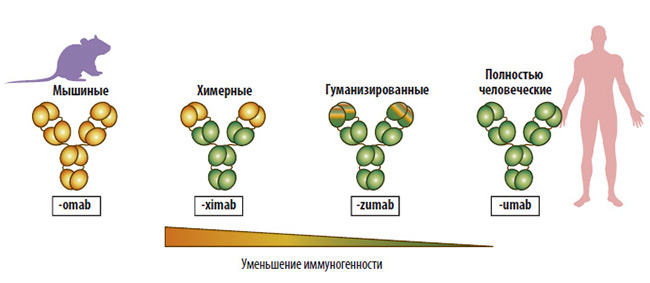
Названия всех моноклональных антител оканчиваются на «–mab» (от Monoclonal AntiBody).
Если антитело получено от мыши, добавляется буква «о», и окончание у таких антител «-omab». Химерные антитела получили окончание «-ximab». Гуманизированные антитела имеют окончание «-zumab», а полностью человеческие «-umab».
Ofatumumab – полностью человеческое моноклональное антитело;
Obinutuzumab — это гуманизированное моноклональное антитело;
Rituximab — это химерное моноклональное антитело.
Производство различных моноклональных антител в настоящее время является наиболее быстро развивающимся сегментом фармацевтической индустрии, составляющим третью часть всех биотехнологических продуктов.
Видео CorMedicale с объяснением работы моноклональных антител – смотреть
При подготовке этой статьи использованы материалы:
“Моноклональные антитела: от создания до клинического применения”. Ю.И. Будчанов, ГБОУ ВПО «Тверской медицинский университет», Тверь, Российская Федерация, 2016 год.